编者按:2019年3月8日至9日中华医学会肿瘤学分会乳腺肿瘤论坛暨首届青年学组年会——南北汇在上海召开,由中华医学会肿瘤学分会乳腺肿瘤学组、复旦大学附属肿瘤医院、上海市抗癌协会等单位共同主办。本届盛会将秉承激发青年创新思维、提高青年创新能力、助力青年创新实践的理念,致力于为青年学者搭建思维碰撞、合作促成、分享交流的平台。会议上讨论内容精彩纷呈,青年学者尽显风采。
 王嘉
王嘉
HER2阳性的pT1micN0乳腺癌是否需要靶向治疗从循证医学角度临床医生是如何认知判断的,经过凝练与思考,来自大连医科大学附属第二医院乳腺疾病研究中心副主任王嘉教授尝试从系统与个体、相对与绝对、指南与共识、理想与现实这四个层次为我们深入解析。
所谓微浸润(microinvasion,pT1mic),即非浸润性乳腺癌的背景下,在乳腺间质内出现1个或多个清晰且独立的肿瘤细胞浸润灶,每个浸润灶最大径均≤1mm。若出现多灶微浸润(2灶或2灶以上),每个微浸润灶需分别测量而不相互叠加。可见,这是一个以大小为基础的定义。
梳理了有关HER2阳性的pT1micN0乳腺癌是否需要靶向治疗的相关研究与指南共识,经过凝练与思考,本文尝试从系统与个体、相对与绝对、指南与共识、理想与现实这四个层次逐次解析。
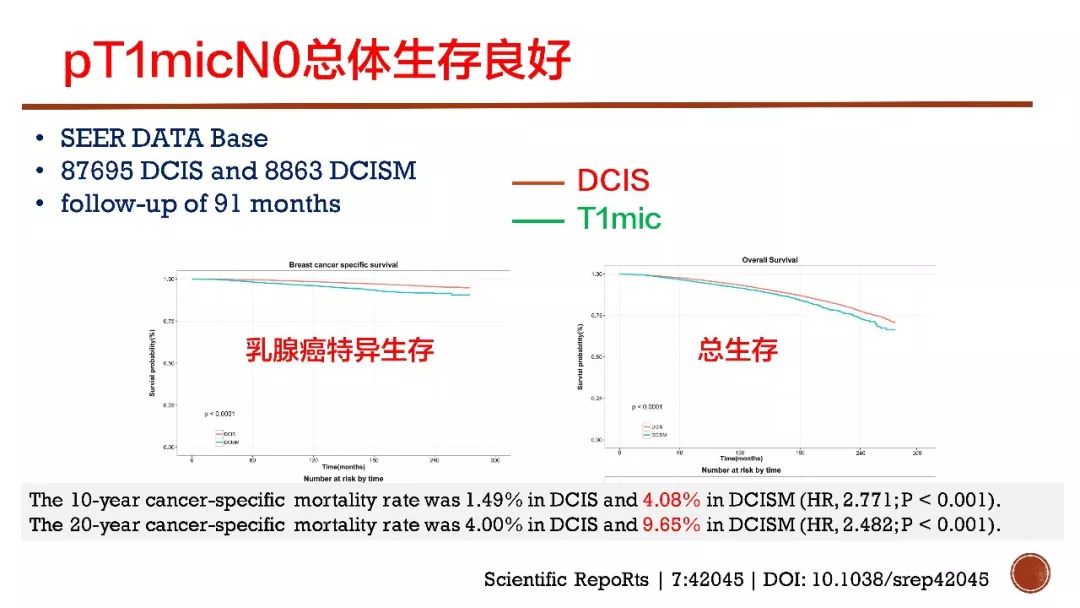
所谓系统与个体,即HER2阳性pT1micN0乳腺癌患者复发转移风险的系统水平与个体水平的表现。据文献报道:分期为pT1micN0者总体生存良好,介于导管原位癌(DCIS)与浸润癌之间;5年无复发生存(RFS)率可以达93%,10年癌症相关性死亡率为4.08%,20年癌症相关死亡率为9.65%。可见这部分患者的总体生存良好。
但检索文献时我们也发现,的确存在一些复发间隔时间短且进展迅速的pT1micN0个案报道。例如,2014年斯洛文尼亚的肿瘤科医生曾经报道过这样一个病例:47岁绝经前女性,广泛DCIS(直径8cm)伴多灶微浸润。行乳房单纯切除和延迟乳房重建术,术后病理示ER<1%、PR-, HER2未行检测,SLNB 0/5(其中两枚存在孤立转移细胞团),患者未接受任何术后辅助治疗。术后8个月因HER2扩增型乳腺癌肝转移,不到半个月死于肝衰竭。此病例虽然罕见,也说明在这群总体生存良好的pT1micN0患者中,确实存在一部分易复发甚至复发后进展凶险的亚群。
有回顾性研究报道称,在未接受辅助化疗与靶向治疗的pT1micN0患者中,HER2阳性者较HER2阴性者预后差。所以,从系统角度看,pT1micN0患者总体生存好,无需靶向治疗;从个体水平看,存在高复发风险人群,例如HER2阳性者。
曲妥珠单抗的靶向治疗已经成为HER2阳性早期乳腺癌辅助治疗的标准治疗手段。证据主要源自NSABP-B31、NCCTG-N9831、BCIRG006、HERA等几项大宗经典的III期随机对照临床试验结果。但这些临床试验基本没有涵盖I期T1a和T1mic人群,仅BCIRG006试验中入组4%左右的小于1cm淋巴结阴性的患者,在这部分亚组分析中我们可以看到,曲妥珠单抗联合化疗组的5年DFS显著优于单纯化疗组(5年DFS:AC->T,AC->TH,TCH/72%,86%,86%)。
以MSKCC等为代表的回顾性分析显示,HER2阳性T1小肿瘤可以从辅助靶向治疗中获益。APT是迄今唯一针对HER2阳性早期小肿瘤前瞻性临床试验。该试验通过非随机单臂设计,旨在为HER2阳性而高危因素较小的患者提供简化的化疗靶向方案。结果显示,这部分患者确实得到了良好的生存结果,3年的DFS率达到98.7%,RFS率为99.2%。细看APT试验中原发肿瘤大小的入组情况,T≤0.5cm入组77名患者,占19%。
综上所述,其实我们并没有直接的证据证明曲妥珠单抗的靶向治疗可以降低HER阳性pT1micN0患者的复发风险,生存收益的可能性很“相对”。相反,1年的曲妥珠单抗这把双刃剑确为患者带来了“绝对”的心脏毒性和经济负担。因此,如何权衡利弊,度长絜大也是临床肿瘤医生值得商榷的课题。
2018ESMO早期乳腺癌国际共识指出:曲妥珠单抗被认可用于淋巴结阳性和N0且T>1cm患者。考虑其相对高复发风险,对于T<1cm N0患者,曲妥珠单抗也可考虑应用,特别是ER阴性患者,证据等级为IV级,推荐等级为B类。St gallen专家共识从2009年开始多次提到HER2阳性早期辅助靶向治疗人群的肿瘤大小问题。2011年的共识对于T1a者无一人支持使用曲妥珠单抗,到2017年已有85.7%的专家投票支持对T1a者使用曲妥珠单抗靶向治疗。但值得注意的是,目前尚无针对pT1micN0者是否需要辅助靶向治疗的专家议题。
最近更新的Version 4. 2018 NCCN乳腺癌指南中,关于HER2阳性小肿瘤的辅助靶向治疗规范中写道:HER2的pT≤0.5cm N0患者可考虑使用周疗紫杉加曲妥珠单抗,特别是ER阴性者,证据等级为2B类。文中特别提到,对于HER2阳性ER阳性的T1mic者复发风险小于5%,内分泌治疗为最佳选择。
综合上述专家共识与指南,可以看出目前尚无关于HER2阳性pT1micN0者从辅助靶向治疗中获益的直接证据,NCCN指南并不推荐对该部分患者行辅助靶向治疗。
大约20-30%早期乳腺癌患者最终发生转移。越来越多的证据显示,转移是肿瘤的固有特性,肿瘤即便1mm时已然存在转移亚克隆,也就是说转移与肿瘤大小无关,是由肿瘤固有分子生物学特性决定的。理论上讲,HER2分子的确可以维持乳腺癌细胞的干性,且曲妥珠单抗或拉帕替尼等小分子TKI可削弱此干性;HERA研究也显示在不同肿瘤大小亚组中曲妥珠单抗治疗与全体人群获益保持一致,不会因为肿瘤小而获益小。
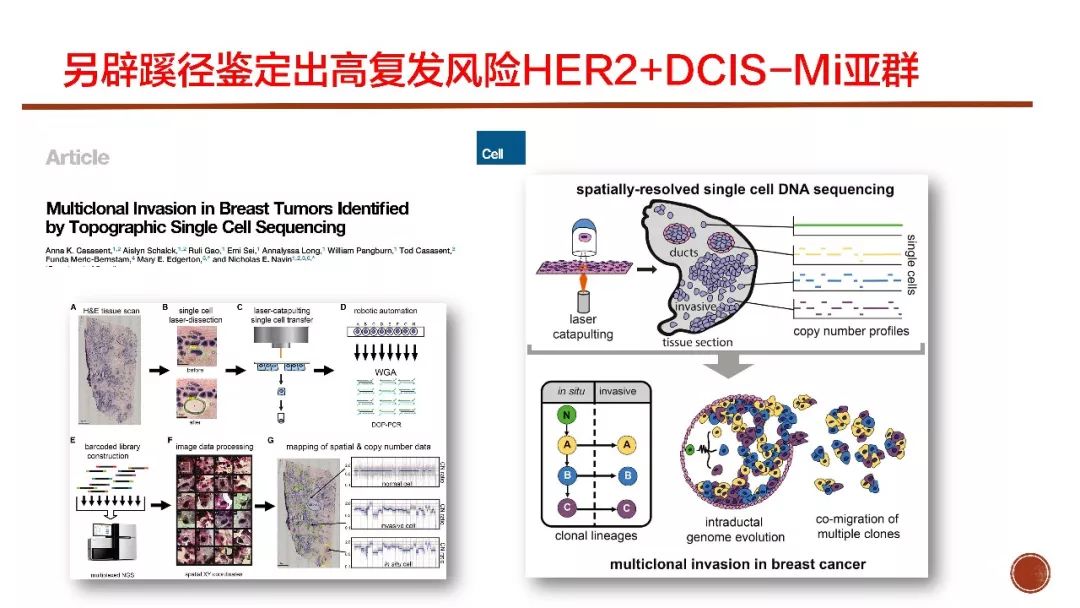
2018SABCS会议上美国MD Andson癌症中心的Navin教授团队做了关于单细胞测序应用于探究乳腺癌进展方面的研究报告。通过显微激光切割与高通量测序技术的结合,绘制出由单个细胞基因突变谱组成的DCIS及浸润癌的整体基因彩绘图,从而推断出乳腺癌的侵袭转移相关克隆已经存在于DCIS阶段,直观的解释了转移是肿瘤的固有特征,决定转移的突变信息已经存在于肿瘤形成的早期。此项技术的临床转化将成为未来连接乳腺癌基础与临床研究的重要桥梁。尤其是与生物信息技术的结合,对本文所述的HER2阳性pT1micN0高复发风险人群的早期预测价值非常值得期待。
现阶段的临床实践中,除了HER2,综合归纳pT1micN0复发风险高者的特征还包括:激素受体阴性、广泛的DCIS、高组织学分级、实性(Solid)或粉刺(Comedo)型改变、多发微钙化、前哨淋巴结中出现孤立转移细胞团及年轻等。综合考虑以上高危因素与患者心脏毒性、经济负担和收益风险,谨慎实践。
总之,对于pT1micN0的HER2阳性乳腺癌患者的靶向辅助治疗:从系统角度看,预后好、复发风险低,且现阶段缺乏循证医学数据,不需要靶向治疗;伴有HR- 、多灶、大面积DCIS、淋巴结见孤立肿瘤细胞等高危因素者结合心毒性与经济收益比可考虑尝试行靶向治疗。通过单细胞测序、生物信息学以及合理的临床试验设计,不远的未来我们将会看到对此课题探索的曙光。

医学博士
大连医科大学附属第二医院乳腺疾病研究中心 副主任
中华医学会肿瘤学分会乳腺学组青委会委员
中国妇幼保健协会青委会委员
中国医药教育协会乳腺病专业委员会委员
中国整形美容协会肿瘤整复分会委员
JCO中文版青年编委
辽宁省细胞生物学学会乳腺肿瘤精准治疗与临床科研专业委员会副主任委员
辽宁省生命科学学会乳腺疾病微创诊断及治疗专业委员会青委会副主任委员
辽宁省生命科学学会乳房整形修复重建与美容专业委员会常务委员





 京公网安备 11010502033352号
京公网安备 11010502033352号